UNIT 5. CHEMISTRY
Text 1. Nomenclature, Physical Properties, and Representation of Structure of Organic Compounds
(by P.Y. Bruice from Essential Organic Chemistry)
If we are going to talk about organic compounds, we need to know how to name them. First, we will learn how alkanes are named because their names form the basis for the names of almost all organic compounds. Alkanes are composed of only carbon atoms and hydrogen atoms and contain only single bonds. Compounds that contain only carbon and hydrogen are called hydrocarbons. Thus, alkanes are hydrocarbons.
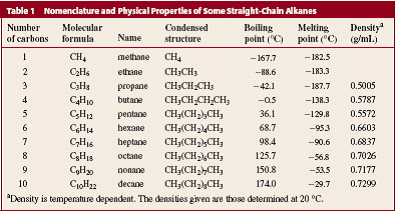
Alkanes in which the carbons form a continuous chain with no branches are called straight-chain alkanes. The names of several straight-chain alkanes are given in the table after the text.
If you look at the relative numbers of carbon and hydrogen atoms in the alkanes listed in the table below (marked as Table 1), you will see that the general molecular formula for an alkane is CnH2n+2, where n is any integer. So, if an alkane has one carbon atom, it must have four hydrogen atoms; if it has two carbon atoms, it must have six hydrogen atoms.
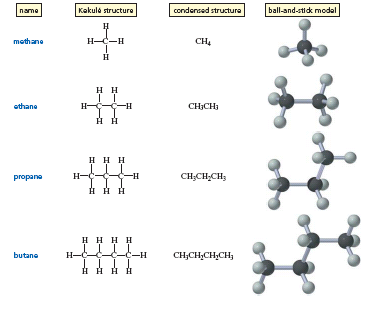
Carbon forms four covalent bonds and hydrogen forms only one covalent bond. This means that there is only one possible structure for an alkane with molecular formula CH4 (methane) and only one structure for an alkane with molecular formula C2H6 (ethane). There is also only one possible structure for an alkane with molecular formula C3H8 (propane).
As the number of carbons in an alkane increases beyond three, the number of possible structures increases. There are two possible structures for an alkane with molecular formula C4H10. In addition to butane – a straight-chain alkane – there is a branched butane called isobutane. Both of these structures fulfill the requirement that each carbon forms four bonds and each hydrogen forms only one bond.
Compounds such as butane and isobutane that have the same molecular formula but differ in the order in which the atoms are connected are called constitutional isomers – their molecules have different constitutions. In fact, isobutane got its name because it is an "iso"mer of butane. The structural unit consisting of a carbon bonded to a hydrogen and two CH3 groups – that occurs in isobutene – has come to be called "iso." Thus, the name isobutane tells you that the compound is a four-carbon alkane with an iso structural unit.
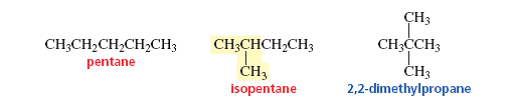
There are three alkanes with molecular formula C5H12. You have already learned to name two of them. Pentane is the straight-chain alkane. Isopentane, as its name indicates, has an iso structural unit and five carbon atoms. We cannot name the other branched-chain alkane without defining a name for a new structural unit.
There are five constitutional isomers with molecular formula С6Н14. Again, we are able to name only two of them, unless we define new structural units.
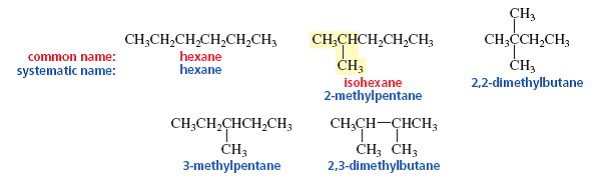
The number of constitutional isomers increases rapidly as the number of carbons in an alkane increases. For example, there are 75 alkanes with molecular formula C10H22 and 4347 alkanes with molecular formula C15H32. To avoid having to memorize the names of thousands of structural units, chemists have devised rules for creating systematic names that describe the compound's structure. That way, only the rules have to be learned. Because the name describes the structure, these rules also make it possible to deduce the structure of a compound from its name.
This method of nomenclature is called systematic nomenclature. It is also called IUPAC nomenclature because it was designed by a commission of the International Union of Pure and Applied Chemistry (abbreviated IUPAC and pronounced "eye-you-pack"). Names such as isobutene – nonsystematic names – are called common names and are shown in red in this text. The systematic (IUPAC) names are shown in blue. Before we can understand how a systematic name for an alkane is constructed, we must learn how to name alkyl substituents.
Alkanes are widespread both on Earth and on other planets. The atmospheres of Jupiter, Saturn, Uranus, and Neptune contain large quantities of methane (CH4), the smallest alkane, an odorless and flammable gas. In fact, the blue colors of Uranus and Neptune are the result of methane in their atmospheres. Alkanes on Earth are found in natural gas and petroleum, which are formed by the decomposition of plant and animal material that has been buried for long periods in the Earth's crust, where oxygen is scarce. Natural gas and petroleum, therefore, are known as fossil fuels.
Natural gas is approximately 75% methane. The remaining 25% is composed of other small alkanes such as ethane, propane, and butane. In the 1950s, natural gas replaced coal as the main energy source for domestic and industrial heating in the United States.
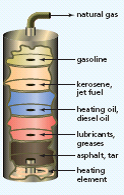
Petroleum is a complex mixture of alkanes that can be separated into fractions by distillation. The fraction that boils off at the lowest temperature (hydrocarbons containing three and four carbons) is a gas that can be liquefied under pressure. This gas is used as a fuel for cigarette lighters, camp stoves, and barbecues. The fraction that boils at somewhat higher temperatures (hydrocarbons containing 5 to 11 carbons) is gasoline; the next fraction (9 to 16 carbons) includes kerosene and jet fuel. The fraction with 15 to 25 carbons is used for heating oil and diesel oil, and the highest boiling fraction is used for lubricants and greases. After distillation, a nonvolatile residue called asphalt or tar is left behind.
Vocabulary
alkane – алифатический углеводород, алкан
carbon – углерод
chain – цепь, цепочка
compound – соединение
constitutional isomer – структурный изомер
covalent bond – атомная связь, ковалентная связь
ethane – этан
fraction – фракция, доля
hydrocarbon – углеводород
hydrogen – водород
integer – целое, единое целое
isobutene – изобутен
isopentane – изопентан
IUPAC – Международный союз теоретической и прикладной химии (ИЮПАК)
methane – метан
nonvolatile residue – нелетучий остаток/ осадок
propane – пропан
single bond – одинарная связь
Exercise 1. Answer the following questions.
- What do we call alkanes?
- What is called a hydrocarbon?
- What kind of alkanes do we call straight-chain ones?
- What is an integer?
- Name the general molecular formula of an alkane.
- What do we call constitutional isomers?
- What does the abbreviation IUPAC stand for?
- Where can we find alkanes?
- H -
- F -
- N -
- Al -
- Cr -
- Mo -
- Fe -
- Sn -
- Ag -
- Au -
- Hg -
- Pb -
- U -
- Pu -
- Zn -
- H -
- F -
- N -
- Al -
- Cr -
- Mo -
- Fe -
- Sn -
- Ag -
- Au -
- Hg -
- Pb -
- U -
- Pu -
- Zn -
Exercise 4. Translate the following sentences from English into Russian/ Belarusian.
- Modern society faces three major problems as a consequence of our dependence on fossil fuels for energy.
- First, these fuels are a nonrenewable resource and the world's supply is continually decreasing.
- Second, a group of Middle Eastern and South American countries controls a large portion of the world's supply of petroleum.
- These countries have formed a cartel known as the Organization of Petroleum Exporting Countries (OPEC), which controls both the supply and the price of crude oil.
- Political instability in any OPEC country can seriously affect the world oil supply.
- Third, burning fossil fuels increases the concentrations of CO2 in the atmosphere; burning coal increases the concentration of both CO2 and SO2.
- Scientists have established experimentally that atmospheric SO2 causes "acid rain," which represents a threat to the Earth's plants and, therefore, to our food and oxygen supplies.
- Since 1958, the concentration of atmospheric CO2 at Mauna Loa, Hawaii has been measured periodically.
- The concentration has increased 20% since the first measurements were taken, causing scientists to predict an increase in the Earth's temperature as a result of the absorption of infrared radiation by CO2 (the greenhouse effect).
- A steady increase in the temperature of the Earth would have devastating consequences, including the formation of new deserts, massive crop failure, decreasing polar ice sheets, and the melting of glaciers with a concomitant rise in sea level.
- Clearly, what we need is a renewable, nonpolitical, nonpolluting, and economically affordable source of energy.
Exercise 5. Translate the following text from Russian into English using the vocabulary and data you have learnt from text 1 in this Unit.
Алканы
(Макарова Н. А. «Органическая химия»)
Алканы (предельные углеводороды, парафины) – насыщенные углеводороды общей формулы СnН2n+2. Простейшим представителем ряда является метан СН4.
Номенклатура. Названия первых четырех алканов – это исто-рически сложившиеся названия. Наименования остальных алканов с не-разветвленной цепью складываются из греческого или латинского названия числительных, соответствующих количеству атомов углерода, и добавления суффикса -ан.
По рациональной номенклатуре все алканы рассматриваются как производные метана, в котором один или несколько атомов водорода замещены на радикал, названия радикалов (в алфавитном порядке) выносятся перед словом метан.
Этапы построения названия алкана по номенклатуре ИЮПАК:
- Найти самую длинную, наиболее разветвленную углерод-углеродную цепь.
- Пронумеровать атомы углерода этой цепи так, чтобы заместители и характеристические группы получили наименьший номер.
- Указать цифрой местоположение заместителя в цепи, назвать заместитель.
- Назвать главную цепь.
Изомерия. В алканах, начиная с бутана, мы сталкиваемся с явлением структурной изомерии. Изомеры – это индивидуальные соединения, имеющие один и тот же состав, но различное строение, т.е. иное расположение тех же атомов в пространстве, а, следовательно, и различные физико-химические свойства.
С увеличением числа атомов углерода в молекулах алканов воз-растает и число структурных изомеров: для гексана оно равно 5, для гептана – 9, для октана – 18, для нонана – уже 35.
В молекулах углеводородов не все атомы углерода равнозначны. Атом углерода, связанный с одним углеродным атомом, называют первичным, с двумя – вторичным, с тремя – третичным, с четырьмя – четвертичным. Все эти атомы различаются по реакционной способности.
СПОСОБЫ ПОЛУЧЕНИЯ
Алканы широко распространены в природе: нефть, попутные нефтяные газы и природный газ, поэтому в промышленных масштабах их выделяют из природного сырья.
Нефть – природное ископаемое, представляющее собой сложную смесь органических веществ, главным образом углеводородов. Состав нефти неодинаков в различных месторождениях, например, некоторые нефти содержат значительные количества ароматических углеводородов.
Нефть содержит как жидкие, так и растворенные в ней твердые и в некотором количестве газообразные углеводороды. При большом содержании последних нефть иногда под давлением газов фонтанирует из буровых скважин.
Нефть – эффективное и дешевое топливо. Кроме того, она является ценным химическим сырьем, на основе которого получают синтетический каучук, пластмассы и т.д.
Крекинг углеводородов. При нагревании углеводородов до высоких температур (450 – 550°С) без доступа воздуха они распадаются с разрывом углеродных цепей и образованием более простых, непредельных углеводородов. Такой процесс называют крекингом (расщеплением). Разложение углеводородов при еще более высоких температурах (550 – 650°С и выше) приводит к образованию простейших (главным образом газообразных) углеводородов; кроме того, при этом происходит замыкание углеродных цепей в циклы и получаются значительные количества ароматических углеводородов. Этот процесс называют пиролизом. Применением в процессах крекинга и пиролиза специальных катализаторов и давления удается регулировать эти процессы и получать необходимые продукты.
Физические свойства. В обычных условиях (при 25°С и ат-мосферном давлении) первые четыре члена гомологического ряда алканов (С1 – С4) – газы, С5 – С15 – жидкости, начиная с C16 – твердые вещества. С ростом числа атомов углерода в соединении возрастают температуры кипения и плавления. Алканы практически не растворимы в воде, хорошо растворимы в неполярных органических растворителях, таких как толуол, бензол, тетрахлорметан и других.
Химические свойства. В обычных условиях алканы химически инертны (русский химик М. И. Коновалов называл предельные углеводороды химическими мертвецами), они не взаимодействуют с концентрированными кислотами и щелочами, не окисляются перманганатом калия и хромовой смесью.
Алканам характерны реакции замещения, протекающие по цепному радикальному механизму, в результате которых атомы водорода в молекуле замещаются на приходящий атом или группу атомов с образованием производных углеводородов.
ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ
Метан СН4 (болотный, рудничный газ) – газ без запаха, растворим в этаноле, эфире, углеводородах и мало растворим в воде (45 мл в 1 л воды при 20°С), является главным компонентом нефтяного и природного газа. Применяется метан как высококалорийное топливо в составе природного газа и как сырье для промышленных синтезов многих продуктов: водорода, ацетилена, хлороформа и других хлорметанов, фреонов, нитрометана, синильной кислоты, синтез-газа. С воздухом образует взрывоопасные смеси, что является причиной взрывов в угольных шахтах. Метан составляет основу атмосферы некоторых планет, например Сатурна, Юпитера.
Пропан С3Н8, бутан С4Н10 – легкосжижаемые газы, используемые в быту в виде баллонного газа. Пропан применяют и как автомобильное топливо, экологически более чистое, чем бензин. Бутан используется для получения бутадиена-1,3, являющегося сырьем для производства синтетических каучуков.
Петролейный эфир – смесь жидких насыщенных алифатических углеводородов (главным образом С5–С6 разветвленного строения), получаемая отгонкой легких фракций бензина. Применяется как растворитель смол, жиров, эфирных масел и других неполярных веществ.
Парафин — смесь твердых алканов C18–С35 (т. пл. 45 – 650 С) преимущественно нормального строения, получаемая из нефти. Представляет собой бесцветный продукт, без запаха и вкуса, жирный на ощупь, нерастворимый в воде и спирте, хорошо растворим в большинстве органических растворителей. Применяется в пищевой промышленности при изготовлении упаковочных материалов, как компонент жевательных резинок, в производстве резинотехнических изделий и товаров бытовой химии. В медицине используют при парафинолечении. Служит сырьем для получения жирных кислот и спиртов, поверхностно-активных веществ.
Вазелин – однородная мазеобразная масса без вкуса и запаха, получаемая расплавлением парафина в минеральном масле. Легко растворяется в углеводородах, в спирте и эфире – при нагревании. Используется в основном для защиты металлических изделий от коррозии.
Вазелин медицинский отличается от технического более высокой степенью очистки и применяется для медицинских, фармацевтических и косметических целей.
1) physical chemistry
2) organic chemistry
3) inorganic chemistry
4) analytical chemistry
5) environmental chemistry
6) green chemistry
7) biochemistry
8) chemical engineering
9) nanotechnology
10) petrochemistry
Exercise 7. Translate the following text from Russian into English and make up an abstract consisting of 3 – 5 sentences.
Фотосинтез
(from «Химическая энциклопедия»)
ФОТОСИНТЕЗ, образование зелеными растениями и некоторыми бактериями орг. веществ с использованием энергии солнечного света. Происходит при участии пигментов (у растений хлорофиллов). В основе фотосинтеза лежат окислительно-восстановительные реакции, в которых электроны переносятся от донора (например, H2O, H2S) к акцептору (CO2) с образованием восстановленных соединений (углеводов) и выделением O2 (если донор электронов H2O), S (если донор электронов, напр., H2S) и др.
Фотосинтез – один из самых распространенных процессов на Земле, обусловливает круговорот в природе углерода, O2 и др. элементов. Он составляет материальную и энергетическую основу всего живого на планете. Ежегодно в результате фотосинтеза в виде органического вещества связывается ок. 8•1010 т углерода, образуется до 1011 т целлюлозы. Благодаря фотосинтезу растения суши образуют ок. 1,8•1011 т сухой биомассы в год; примерно такое же количествово биомассы растений образуется ежегодно в Мировом океане. Тропический лес вносит до 29 % в общую продукцию фотосинтеза суши, а вклад лесов всех типов составляет 68 %. Фотосинтез высших растений и водорослей – единственный источник атм. O2.
Возникновение на Земле ок. 2,8 млрд лет назад механизма окисления воды с образованием O2 представляет собой важнейшее событие в биол. эволюции, сделавшее свет Солнца главным источником свободной энергии биосферы, а воду – практически неограниченным источником водорода для синтеза веществ в живых организмах. В результате образовалась атмосфера современного состава, O2 стал доступным для окисления пищи, а это обусловило возникновение высокоорганизованных гетеротрофных организмов (применяют в качестве источника углерода экзогенные органические вещества).
Около 7 % органических продуктов фотосинтеза человек использует в пищу, в качестве корма для животных, а также в виде топлива и строительного материала. Ископаемое топливо – тоже продукт фотосинтеза. Его потребление в конце XX в. примерно равно приросту биомассы.
Общее запасание энергии солнечного излучения в виде продуктов фотосинтеза составляет ок. 1,6 • 1021 кДж в год, что примерно в 10 раз превышает современное энергетическое потребление человечества. Примерно половина энергии солнечного излучения приходится на видимую область спектра (длина волны l от 400 до 700 нм), которая используется для фотосинтеза (физиологически активная радиация, или ФАР). ИК-излучение не пригодно для фотосинтеза кислородовыделяющих организмов (высших растений и водорослей), но используется некоторыми фотосинтезирующими бактериями.
Exercise 8. Translate the following abstracts into Russian/ Belarusian.
1) Chemoselective Reduction of the Carbonyl Functionality through Hydrosilylation: Integrating Click Catalysis with Hydrosilylation in One Pot
S. R. Roy, S. C. Sau, S. K. Mandal, J. Org. Chem., 2014, 79, 9150-9160.
Abstract
A chemoselective reduction of the carbonyl functionality via hydrosilylation using low loadings of a copper(I) catalyst bearing an abnormal NHC takes place at ambient temperature in excellent yield within a very short reaction time. The hydrosilylation reaction of α,β-unsaturated carbonyl compounds gives allyl alcohols in good yields. The catalyst can also be used for azide-alkyne cycloadditions.
Key Words
reduction of carbonyl compounds, phenylsilane
2) A New Iron (III)-Salen Catalyst for Enantioselective Coniaene Carbocyclization
S. Shaw, J. D. White, J. Am. Chem. Soc., 2014, 136, 13174-13177.
Abstract
A chiral iron(III)-salen complex catalyzes an asymmetric Conia-ene-type cyclization of α-functionalized ketones containing an unactivated terminal alkyne and produces an exo-methylenecyclopentane scaffold possessing a stereodefined quaternary center.
Key Words
Conia-ene reaction, Cyclopentanes
3) Cobalt-Catalyzed Vinylation of Aromatic Halides Using β-Halostyrene: Experimental and DFT Studies
A. Moncomble, P. Le Floch, A. Lledos, C. Gosmini, J. Org. Chem., 2012, 77, 5056-5062.
Abstract
A direct cobalt-catalyzed vinylation of various aromatic halides using β-halostyrene proceeded smoothly with a total retention of the double bond configuration in the presence of triphenylphosphine as ligand. This procedure offers a new route to the stereoselective synthesis of functionalized stilbenes.
Key Words
Stilbenes, Manganese
Exercise 9. Translate the following abstracts of scientific articles into English.
ЕЖЕГОДНИК
УСПЕХИ БИОЛОГИЧЕСКОЙ ХИМИИ
АННОТАЦИИ СТАТЕЙ (т. 42)
1) И. Н. Сердюк Физичeскиe мeтоды в структурной молeкулярной биологии в начале ХХI вeка
За годы, прошедшие после открытия двойной спирали ДНК, физики разработали ряд новых мeтодов, позволивших изучать структуру биологичeских макромолeкул с разным пространствeнным разрeшeниeм: от низкого, соответствующего размерам целой молекулы, до высокого, соответствующего расстояниям между отдельными атомами в молекуле. Это позволило окончательно сформировать науку, получившую название структурной биологии. В 80-х годах ее плавное развитие было прервано двумя революционными событиями. Первое из них произошло в физике и связано, в первую очередь, с появлением синхротронных источников и быстродействующих рентгеновских детекторов. Их применение в рентгеноструктурном анализе привело к тому, что число расшифрованных белковых трехмерных структур стало быстро расти. Другое событие произошло в биологии, когда было показано, что послeдоватeльность аминокислотых остатков бeлка гораздо быстрee можно опрeдeлить по послeдоватeльности eго ДНК. Эти два события создали условия для появления новой ветви структурной биологии, структурной геномики – науки, главной задачей которой является определение в атомарном разрешении набора трехмерных структур белков, кодируемых данным геномом. Ее дальнейшим развитием является функциональная протеомика, одной из задач которой является изучение на молекулярном уровне фенотипа организма, то есть свойств организма, вытекающих из комбинации его генотипа и факторов окружающей среды.
В данном обзоре в сжатой форме описано прошлое и современное состояние физических методов, обсуждаются тенденции их развития. Говоря о будущем этих методов, надо всегда помнить, что перспективы их развития не отделимы от перспектив развития компьютеров, электроники, лазеров, оптики, нейтронных и синхротронных источников.
2) М. В. Хоретоненко, Е. А. Рудакова, М. Г. Ивановская Современные методы изучения РНК-полимеразы E. coli
РНК-полимераза E.coli отвечает за транскрипцию в бактериальных клетках. В настоящее время накоплено большое количество данных, касающихся механизма действия и структурно-функциональной характеристики этого фермента, которые свидетельствуют о том, что процесс транскрипции в E.coli во многом сходен с процессом транскрипции в других, в том числе и эукариотических клетках. Поэтому РНКП E.coli остается объектом пристального изучения. Наряду с традиционными биохимическими методами изучения транскрипции в настоящее время широко используются новые физические и физико-химические подходы. В обзоре рассматриваются основные физико-химические и новые физические методы исследования белково-нуклеиновых взаимодействий на примере комплекса РНКП E.coli с промотором. Наряду с широко распространенными методами, такими, как рентгено-структурный анализ, флуоресценция, футпринтинг, обсуждаются и новые: метод резонансного переноса энергии возбуждения флуоресценции, кросслинк, новейшие варианты электронной микроскопии и т.д. Приведена оценка возможностей и ограничений указанных методов, а также некоторые данные по структуре и функции промоторного комплекса РНКП E.coli.
3) А. Д. Никулин Изучение взаимодействий рибосомных белков с рибосомными РНК
В обзоре рассмотрены имеющиеся на середину 2001 года модели рибосомы и рибосомных субчастиц, полученные как электронно-микроскопическими методами, так и рентгеноструктурными методами. Дан краткий анализ моделей рибосомных субчастиц. Показано, что полученные модели рибосомы и рибосомных субчастиц содержат довольно большую ошибку в координатах атомов, что не позволяет с достаточной точностью проанализировать взаимодействия рибосомных белков и рРНК между собой. Кроме того, структуру не всех участков рибосомы удается определить даже при наличии карт электронной плотности высокого разрешения. Поэтому в настоящее время большое внимание уделяется структурным исследованиям сравнительно небольших комплексов рибосомных белков со специфично связывающимися фрагментами рРНК. Для таких комплексов можно получить кристаллы, дающие дифракционные картины высокого разрешения, определить структуры комплексов с высокой точностью и детально проанализировать РНК-белковые взаимодействия, что также позволяет восполнить пробелы в структуре рибосомы. Проведен анализ полученных к настоящему времени моделей структур комплексов рибосомных белков с рРНК и сделан ряд предварительных выводов относительно принципов РНК-белковых взаимодействий.
4) Б. И. Курганов Оценка активности молекулярных шаперонов в тест-системах, основанных на подавлении агрегации белков
Функция молекулярных шаперонов состоит в том, что, взаимодействуя с развернутыми состояниями белковой молекулы, они препятствуют их агрегации и обеспечивают, таким образом, возможность сворачивания полипептидной цепи в нативную структуру. Оценка эффективности действия шаперонов в тест-системах, основанных на подавлении агрегации белковых субстратов, требует понимания механизма агрегации белков. В обзоре обсуждаются кинетические режимы агрегации белков. Проведенный автором обзора анализ кинетики агрегации белков показывает, что в большинстве случаев протекающая во времени агрегация после прохождения лаг-фазы следует кинетике реакции первого порядка. Разработаны подходы, позволяющие количественно оценить эффективность подавления агрегации белкового субстрата шапероном.
5) А. С. Воронина Трансляционная регуляция в раннем развитии
Вниманию читателей представляется обзор совокупности данных по регуляции трансляции на запасенных мРНК в оогенезе, эмбриогенезе и в дифференцированных тканях. Рассмотрена роль нетранслируемых областей мРНК, с которыми связываются определенные белки, регулирующие функционирование индивидуальных мРНК. Описаны примеры пространственной и временной регуляции трансляции индивидуальных мРНК в эмбриогенезе.
6) Н. М. Груздева, А. П. Куллыев Инсуляторы Drosophila melanogaster: структура, функции
Несмотря на множество имеющихся данных о регуляции транскрипции, механизм взаимодействия между регуляторными элементами остается неясным. Недавние исследования взаимодействий между энхансером и промотором на больших дистанциях позволили объединить регуляторные элементы в единую систему, в результате работы которой осуществляется контроль над экспрессией генов. В обзоре излагаются современные представления об инсуляторах как элементах, регулирующих взаимодействия между энхансерами и промоторами. На основе предложенной ранее модели, основывающейся на взаимодействии между инсуляторами, излагается возможный механизм регуляции транскрипции в локусе Abd-B.
7) В. А. Костюченко, В. В. Месянжинов Архитектура сферических вирусов
Простейшие капсиды сферических вирусов, состоящие из идентичных копий продукта одного гена, построены на основе икосаэдрической симметрии с идентичными (эквивалентными) взаимодействиями субъединиц, и представляют генетически экономичный способ формирования оболочки для упаковки и хранения вирусного генома. Капсиды вирусов, построенные более чем из 60 копий одного или нескольких продуктов генов, благодаря конформационной гибкости молекул белка, способных формировать в поверхностной решетке капсида различные олигомеры, как, например, гексамеры и пентамеры, обладают квазиэквивалентными взаимодействиями субъединиц в поверхностной решетке. Для сборки сложных капсидов с нарушениями квазиэквивалентности необходимы вспомогательные белки, как, например, внутреннее ядро у ДНК-содержащих фагов, таких как фаг Т4 и вирус герпеса. Вокруг ядра собирается прокапсид, ядро удаляется с помощью протеолиза, а затем в капсид упаковывается геномная ДНК вируса. Принципы ассоциации субъединиц белка и регуляции сборки вирусов реализуются во многих биологических структурах и процессах клетки.
8) Т. А. Валуева, В. В. Мосолов Роль ингибиторов протеолитических ферментов в защите растений
В процессе эволюции растения выработали механизмы, позволяющие им успешно противостоять неблагоприятным воздействиям, в том числе, различного рода вредителям и патогенным микроорганизмам. Важнейшими компонентами подавляющего большинства таких механизмов являются вещества белковой природы. Среди них важную группу составляют ингибиторы ферментов и, в первую очередь, ингибиторы протеаз. В обзоре анализируются имеющиеся в литературе и собственные данные о различных формах участия ингибиторов протеолитических ферментов в защите растений. Рассмотрено действие ингибиторов протеиназ из растений и некоторых других источников на ферменты насекомых, нематод, фитопатогенных микроорганизмов и вирусов. Значительное внимание уделено процессам индукции ингибиторов протеиназ у растений в ответ на поражение насекомыми и микроорганизмами. Рассмотрены также выработанные насекомыми в процессе эволюции способы нейтрализации действия ингибиторов протеиназ, содержащихся в растениях. В обзоре затрагиваются некоторые аспекты применения ингибиторов протеиназ в биотехнологии для получения трансгенных растений, характеризующихся повышенной устойчивостью к вредителям и болезням.
9) А. С. Костюкова Структура и функции тропомодулина, белка, регулирующего длину актиновых филаментов
Тропомодулин (40 кДа) – это уникальный белок, кэпирующий актиновые филаменты на медленно растущем (остром) конце и тем самым определяющий их длину. Структура и функции N- и C-концевых половин тропомодулина различны. C-концевая половина определяет кэпирующие свойства тропомодулина и, по-видимому, взаимно. Описаны примеры пространственной и временной регуляции трансляции индивидуальных мРНК в эмбриогенезе.
10) Е. В. Кудряшова, А. К. Гладилин, А. В. Левашов Белки (ферменты) в надмолекулярных ансамблях: исследование структуры методом разрешенно-временной флуоресцентной анизотропии
Надмолекулярные структуры играют важную роль в таких ключевых биохимических процессах, как фолдинг белков, транспорт разнообразных соединений, биосинтез и многих других. Регуляция каталитической активности и стабильности ферментов in vivo часто осуществляется посредством образования надмолекулярных ансамблей с веществами различной природы. B обзоре рассмотрены белок-содержащие нековалентные комплексы с основными классами природных и синтетическиx соединений и физико-химическиe методы исследования структуры таких комплексов. Подробно обсуждаются флуоресцентные методы анализа. Одним из наиболее информативных при исследовании структуры надмолекулярных ансамблей является метод разрешенно-временной флуоресцентной анизотропии, позволяющий следить за вращательной динамикой как всего комплекса, так и его отдельных фрагментов. Благодаря высокой чувствительности метод позволяет получить детальную информацию о структурной организации надмолекулярных ансамблей.
